临床实践 l 2023严重低钠血症的急诊处理(全/O)
时间:2024-02-17 15:13 来源:CK医学Pro 作者:陈康 编/译 点击:次
在临床实践中,低钠血症的病因往往是多因素的,在单次发生的治疗过程中,可能需要对治疗方法进行调整优化。因此,定期重新评估临床状态和生化非常重要,同时要警惕潜在病因,这些因素在治疗过程中可能会变得更加明显。 在没有需要紧急干预的严重症状的情况下,液体限制(FR)在当前指南中被广泛认可为SIAD的一线治疗,但在FR不成功的情况下(约有一半的病例出现这种情况),二线治疗存在相当大的争议。 本系列回顾
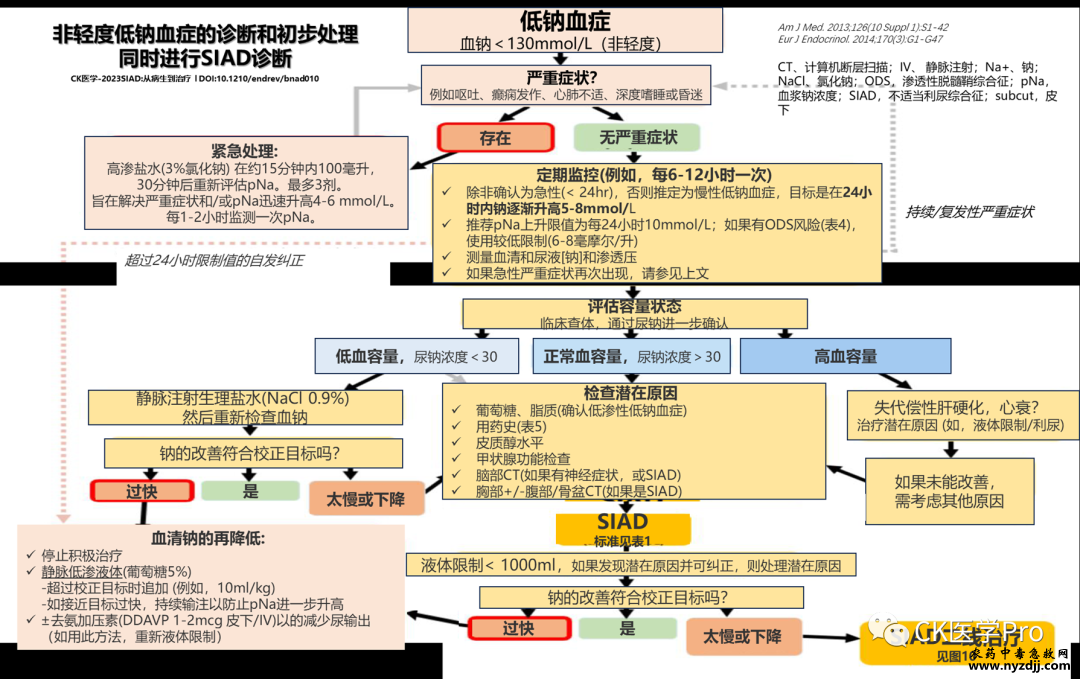
系列前述内容可见: 本部分主要涉及急症的快速评估和治疗,这是难点。 有关SIAD相关进展和更细节的内容: 陈康 临床实践 l 2023 严重低钠血症的急诊处理 编译/陈康 低钠血症的初始治疗包括评估神经系统症状和体征,以确定是否是需要使用高渗盐水紧急治疗重度低钠血症(图1)。重度低钠血症可能导致脑水肿,从而导致癫痫发作、昏迷或死亡。
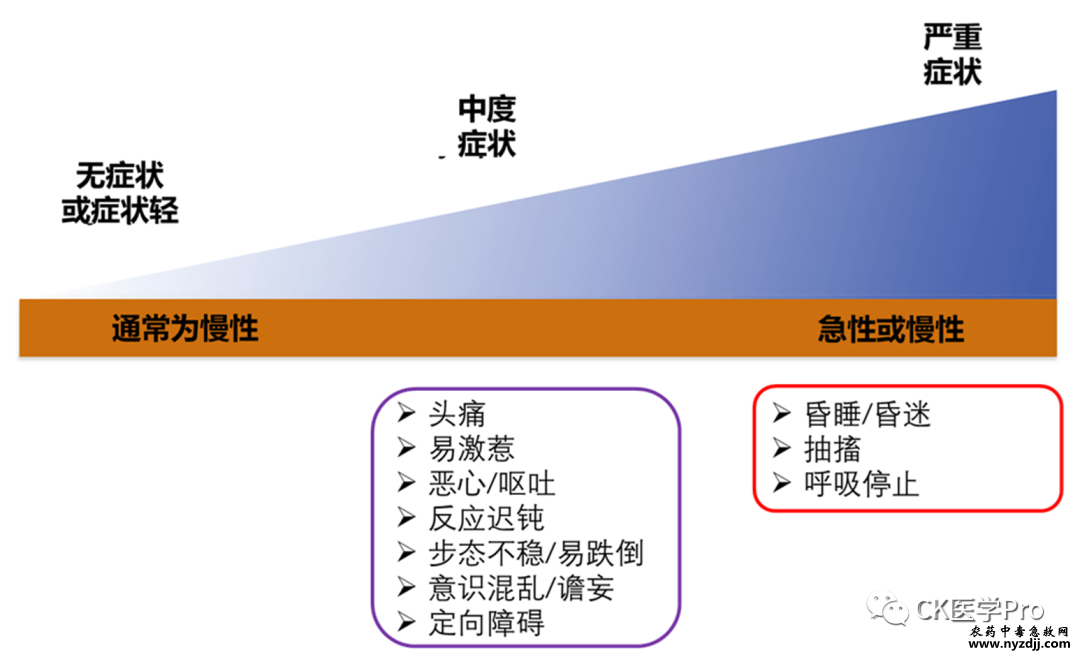
急性重度低钠血症 急性重度低渗性低钠血症属于医疗急症。由于水渗透流入大脑,可导致脑水肿,导致受限颅骨内ICP升高,以及潜在的脑疝和死亡(参见图2)【Front Horm Res. 2019;52:36-48】。 图2 低钠血症急性发生与慢性发生发展示意图 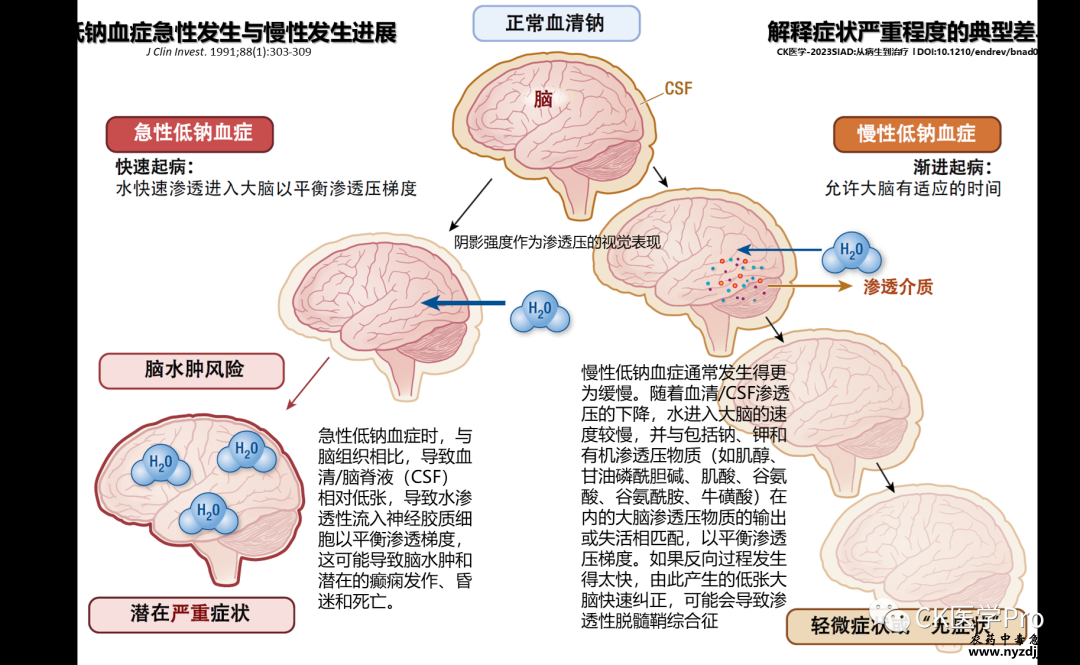 指征即将发生的不良结果的“严重”症状可能包括呕吐、癫痫发作、嗜睡(GCS评分< 8)、昏迷或ICP(库欣反射)增加的心肺表现,如心动过缓、脉压增宽和呼吸不规则【NEJM. 1986;314(24):1529-1535】。严重症状的存在需要紧急干预,参见“严重低钠血症的紧急处理”部分其它内容。在此之前可能出现的中度严重症状包括恶心、意识模糊和头痛【EJE. 2014;170(3):G1-G47】。可能发生快速进展,特别是在急性水摄入的情况下(此时胃中有水仍有待吸收),或在不适当的低渗IV液体给药的情况下。
这些汇总数据支持对严重症状性低钠血症(通常使用大剂量高渗盐水)进行干预,认为这对于改善发病率和死亡率至关重要(参见“严重低钠血症的紧急处理”部分)。 生化和症状严重程度并不总是很好地相关,因为慢性低钠血症患者由于大脑适应可能具有非常低的血清钠浓度但伴较轻症状,然而血清钠急性急剧下降(即使仍在120 mmol/L以上的浓度)的患者可能表现出严重的症状【Ann Intern Med. 1992;117-(11):891-897】。 出现严重症状时,应根据已发表病例中观察到的临床改善情况,使用谨慎的高渗盐水推注进行及时治疗,目标是血清钠增加4至6 mmol【Semin Nephrol. 2009;29(3):282-299】。
总体而言,这些研究说明在有症状的低钠血症中使用高渗盐水积极干预以降低ICP并改善并发症发生和死亡率的基本原理。
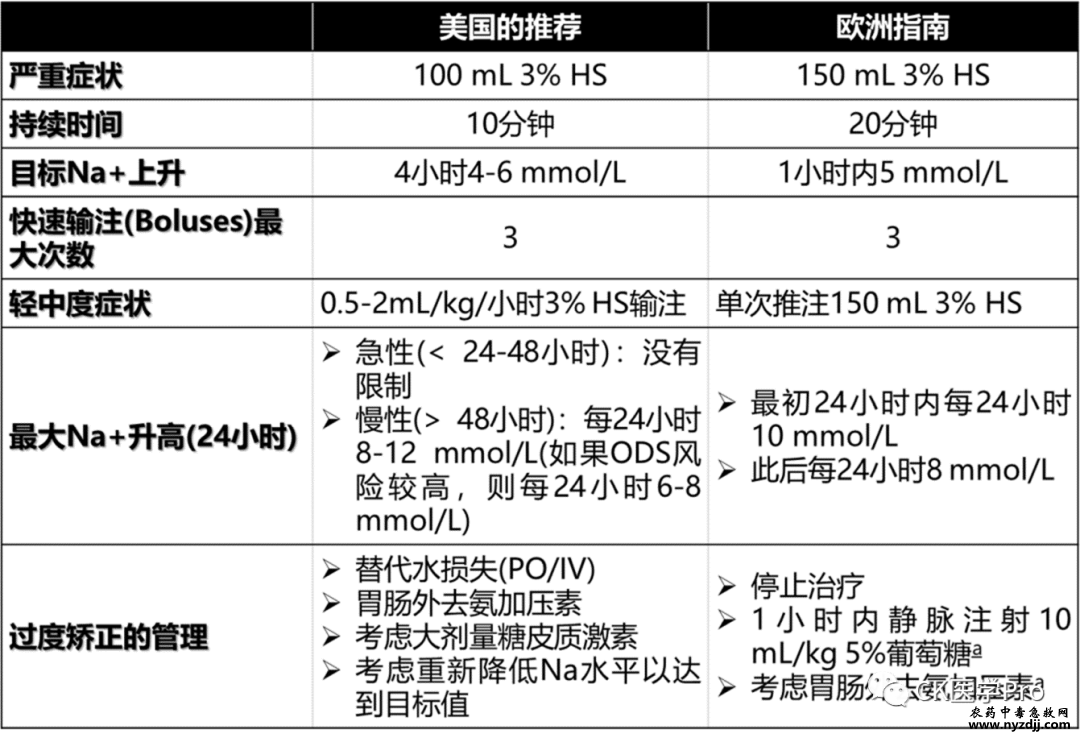
尽管“急性”低钠血症发生的常规界限被认为是48小时,但在临床上,有专家赞成更保守的小于24小时定义,前提是在允许快速纠正之前,这一定义需经病理学结果证实,以最大限度地降低ODS风险。 急症低钠早期处理 如果出现急性重度低钠血症的情况建议紧急干预,在约15分钟内输注100mL高渗(3%)氯化钠。初始剂量之后应进行临床重新评估,如果无临床反应,则重复给药,直至达到目标增量【JCEM.2019;104(9):3595-3602】(图3)。目标是使初始钠浓度增加4-6 mmol。2014欧洲指南中关于严重症状低钠血症的推荐见图4。
根据Adrogué-Madias公式估计液体给药对pNa的影响,在大多数平均身高(50-80 kg)的成人中,100 mL含51.3 mmol Na+的3% NaCl预计会使血清钠增加1至1.5 mmol/L(假设在同一时间间隔内无尿无电解质水清除)【NEJM. 2000;342(21):1581-1589;QJM. 2003;96(8):549-552】 (见图5)。  Cr,肌酐;FEUA,尿酸排泄分数;mOsm,毫摩尔;Na+,钠;UA, 尿酸。 【Am J Med. 1999;106(4): 399-403】 【Intensive Care Med. 1997;23(3):309-316】 【Am J Kidney Dis. 1998;32(6):917-933】 高渗盐水是首选药剂,因为它可立即生效并可滴定;它将可靠地增加血清钠,而独立于潜在病因,至少在开始时如此,因为它的渗透压(1026 mOsmol/L)超过了最大尿渗透压。不建议在急性严重症状消退后继续使用高渗盐水,因为存在血清钠过度校正的风险,约20%的病例可能发生这种情况(除非低钠血症的急性持续时间< 24小时,且可耐受快速校正)(参见前述“急性严重低钠血症”和图2) 【JCEM.2019;104(9):3595-3602;Am J Med. 2016;129(5):537.e9-553.e23】。如果给药超过2次100 mL,或超过一次150mL 3% NaCl,矫正过度的风险明显更高【JCEM.2019;104(9):3595-3602;JAMA Intern Med. 2021;181(1):81-92】。早期已经认识到,高渗盐水在SIAD不一定具有长期的治疗效果,因为使用的钠最终将通过尿液排出【NEJM. 1961;264:67-72;Am J Med. 1957;23(4):529-542;Am J Med. 1967;42(5):790-806】;然而,它的直接功效可能是拯救生命。 高渗盐水通常在高依赖性环境(high-dependency setting/监护条件下)或紧急复苏舱(emergency resuscitation bay)中给药,以便进行密切监测。通过外周或中心静脉给予NaCl是安全的【Crit Care Nurse. 2021;41(1):25-30】。尽管如此,一些给药方案错误地要求使用中心静脉或对3%氯化钠的使用进行其他限制,以及如需要ICU。由于流程障碍导致的高渗盐水延迟可能会产生致命的后果【Front Med (Lausanne). 2019;6:47】。为了应对这些限制,有时会使用替代方法来规避这些要求,例如,在美国的一些医院中,使用2%高渗盐水而不是3%。然而,2% NaCl (684 mmol/L)的渗透压浓度并不可靠地高于尿液的最大浓度,其使用可能会延迟症状的改善;因此,并非3%氯化钠的良好替代品。有专家建议修订与当前最佳实践不同的基于非证据的方案,以便在任何医院环境中通过适当的监测促进3% NaCl的外周给药和紧急给药,而不是建议变通的其他替代治疗。有关美国与欧洲建议/指南对急性或症状性低钠血症治疗的不同见下表1。
预防渗透性脱髓鞘综合征(ODS) 在慢性或持续时间未知的低钠血症中,一个至关重要的考虑因素是通过避免过快纠正血清钠浓度来管理ODS的风险,血清钠浓度的过快纠正会因渗透应激而损害保护性神经髓鞘,并产生严重的、潜在致命的后果。 ODS 最早于1959年报告,在一病例系列表现为快速发展的弛缓性四肢瘫痪、假性球麻痹,然后在数周内死亡的患者中,这些患者在尸检时被发现有明显的脑桥病变,其背景为酗酒和营养不良【AMA Arch Neurol Psychiatry. 1959;81(2): 154-172】。直到20世纪80年代,在动物中进行的临床前研究证明慢性低钠血症快速纠正后脱髓鞘后,才确定原因【Science. 1981;211(4486):1068-1070】,由一致的患者观察结果支持【NEJM. 1986;314(24):1535-1542】。 慢性低钠血症时,脑细胞通过降低细胞内渗透压(如电解质[钠、钾、氯]和非电解质有机渗透压)来适应降低的血清张力。这降低了脑组织和血清之间的张力梯度,减少了水流入量并降低了脑水肿的风险(图6)。 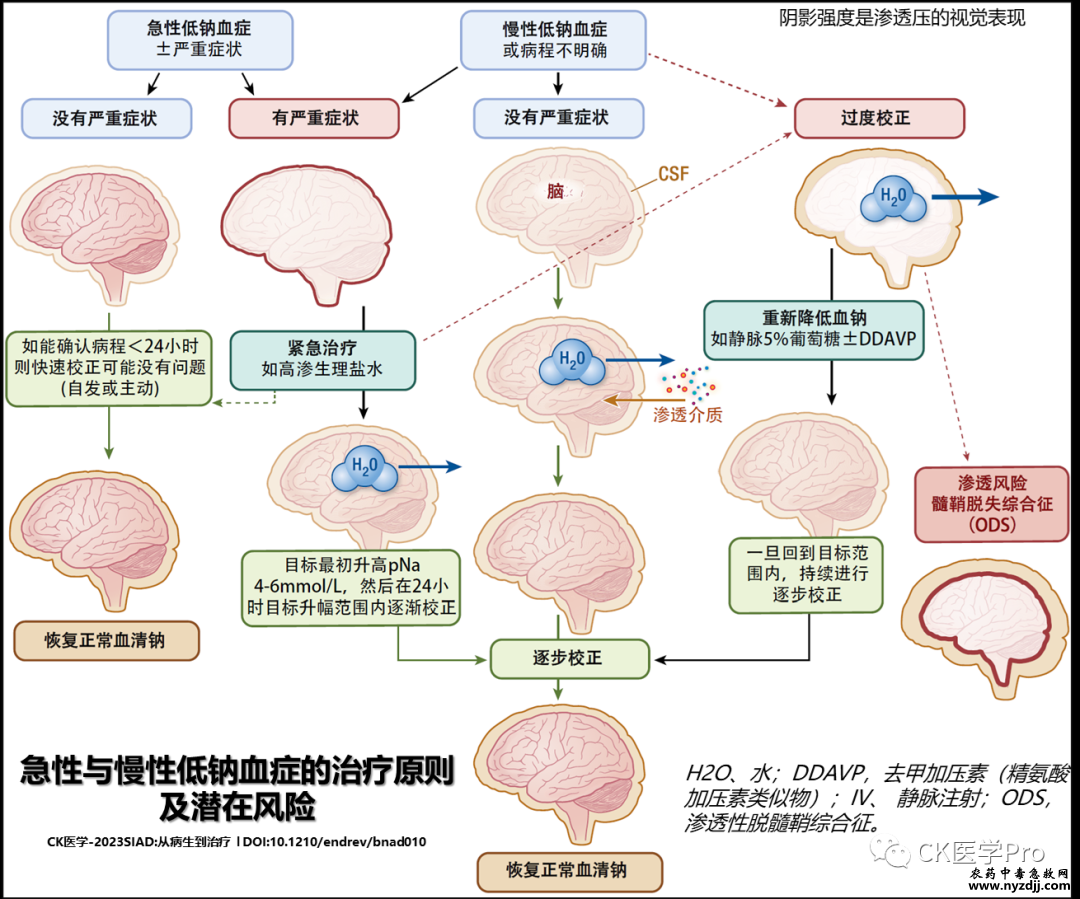 阴影强度是渗透压的视觉表示。在急性低钠血症中,尚未发生脑渗透压适应,因此允许(或诱导)快速纠正血清钠是可以接受的,且ODS的风险较低。有专家主张将低钠血症持续时间的界限从48小时缩短至24小时,以最大限度地提高该方法的安全性。对于出现任何(或未知)持续时间的严重症状的低钠血症,需要使用大剂量高渗盐水进行紧急处理,以防止出现可能危及生命的脑水肿(参见“严重低钠血症的紧急处理”)。一旦达到血清钠升高的目标初始增量(如4-6 mmol/L)和/或症状改善,则根据低钠血症的持续时间确定持续纠正。如果持续时间未知,最安全的方法是推定为慢性,并以逐渐纠正为目标。在慢性低钠血症中,通过导入或合成渗透压调节剂(钠、钾、有机渗透压调节剂,如前图2所述),逐渐纠正血清钠可使脑组织渗透压恢复至正常范围以及过量细胞内水的缓慢排出。典型的目标校正率为每24小时5-8 mmol/L,对于具有ODS风险因素的患者,校正率更低。如果出现高于目标速率的血清钠快速纠正(纠正过度,如> 10 mmol/L,在24小时内),建议重新降低血清钠以预防ODS的罕见并发症,如静脉注射5%葡萄糖和/或去氨加压素(DDAVP),参见下文“纠正过度:重新升高血浆钠”。ODS可作为细胞内水快速排出的结果发生,破坏髓鞘,特别是脑桥中的髓鞘,并可导致破坏性神经后果或死亡。ODS症状的出现通常会延迟。重新降低后的后续纠正应是渐进的。
大脑适应的程度是区分“急性”和“慢性”低钠血症的基础,通常定义为低于或高于48小时的持续时间,因为慢性低钠血症被认为已经存在足够长的时间,以至于电解质和有机渗透压物质都耗尽而发生——但实际上,这是一个逐渐的连续过程。纠正低钠血症后,脑电解质浓度的恢复比有机渗透压调节剂快得多,后者可能需要5天才能恢复到基线水平,通常是重新合成的【JCI. 1991;88(1):303-309;Brain Res. 1993;606(1):19-27】。慢性低钠血症的逐渐纠正为安全逆转适应过程提供了足够的时间。 慢性低钠血症纠正过快意味着血清和脑脊液(CSF)(即细胞外)张力的增加速度超过脑细胞内张力的上升速度,特别是考虑到有机渗透压介质无法迅速恢复【JCI. 1991;88(1):303-309】。这导致水从低渗脑细胞中渗透出来,随后神经元脱水导致细胞皱缩(皱缩和表面畸形)。这又导致细胞连接和血脑屏障的破坏,导致少突胶质细胞损伤和神经元脱髓鞘【Nat Rev Neurosci. 2006;7(1): 41- 53】。保护轴突的髓鞘由少突胶质细胞的足突组成,由维持稳态并形成血脑屏障的星形胶质细胞支持。这些神经胶质细胞(星形胶质细胞、少突胶质细胞)被认为最易受快速钠纠正引起的渗透损伤的影响,因为它们形成脑细胞和负责水交换的CSF之间的界面,并含有高浓度的水通道蛋白【J Am Soc Nephrol. 2011;22(10):1834-1845】。这也可能意味着它们可能变得比其它细胞相对更耗尽有机渗透物。神经胶质细胞的另一个易损性因素是低钠血症已被证明可下调少突胶质细胞中普遍存在的中性氨基酸转运体,该转运体对渗透适应很重要【Neuroscience. 2008;153(1):95-107】。脱髓鞘的确切病理生理学尚不完全清楚,但齿状回的联合损伤和细胞内阳离子(钠、钾)的流入(以补偿有机渗透剂的缺乏)会导致蛋白质聚集和DNA片段化,从而促进细胞凋亡。渗透损伤后约24小时,星形胶质细胞和少突胶质细胞开始死亡。ODS造成的髓鞘损伤通常在脑桥中最为明显(因此,以前称为脑桥中央髓鞘溶解症),但脑桥外髓鞘溶解症可影响其他区域,如基底神经节和丘脑,约有10%的病例【NEJM. 1986;314(24):1535-1542】。脑桥富含白质,比大脑的其他部分具有更高的表面积与体积比。动物研究中观察到,与脑的其他区域相比,脑桥附近的中脑和纹状体在慢性低钠血症后表现出较慢的有机渗透物恢复,这也可以解释这些区域脱髓鞘病变更明显【JCI. 1995;95(4):1579-1586】。这可能是由于脑桥中有机化合物的血脑屏障通透性较低,因为研究表明该区域的药物浓度低于大脑的其他区域【Comp Med. 2013;63(4):355-360】,推测可能对控制呼吸等基本功能的这一关键区域具有对抗毒素的保护作用【Front Oncol. 2018;8:239】。 ODS的症状通常以延迟的方式出现,即在过度纠正发生后一天或多天。临床上,随着pNa的升高,有严重症状的低钠血症患者最初可能会得到改善;然而,随着ODS发生,随后可能会出现进行性、有时是永久性的神经系统恶化。 ODS症状包括构音障碍、吞咽困难、松弛性四肢瘫痪(随后变为痉挛)、水平凝视麻痹、“闭锁/Locked-in”综合征和昏迷【NEJM. 1986;314(24):1535-1542】。与脑桥外髓鞘溶解症相关的临床特征包括震颤、共济失调、帕金森综合征、肌张力障碍和紧张症。迄今为止最大的两个当代病例系列(瑞典83例和美国45例ODS患者)报告的住院死亡率分别为7.2%和13%【Acta Neurol Scand. 2019;140(5):342-349;Neurol Clin Pract. 2021;11(4):304-310】。随访3至6个月后,约60%的患者功能恢复,而其余存活者存在持续的功能障碍。 除极低的初始钠浓度(如< 105 mmol/L)和快速纠正(如> 12 mmol/L,24小时内)外,ODS的风险因素包括低钾血症、酗酒、营养不良和晚期肝病(表2)【 Clin J Am Soc Nephrol. 2019;14(7):975-982;Indian J Crit Care Med. 2013;17(4):231-233】。这些因素可能会削弱神经胶质细胞导入或重新合成有机渗透物质的能力【Clin Exp Nephrol. 2015;19(3): 489-495】。低钾血症时内皮细胞膜Na-K-ATP酶浓度降低也可能损害电解质的转运,进一步使神经胶质细胞易于受到与血清钠浓度快速升高相关的损伤【Am J Med. 1994;96(5):408-413】。
尽管过度矫正的情况相对频繁,但ODS相对较少。在最近一项对1490例pNa在16年间低于120 mmol/L的患者进行的回顾性研究中,41%的患者在24小时内pNa升高超过8 mmol/L,但只有9例(0.5%)患者通过磁共振成像记录了ODS(除1例患者外,所有患者均至少存在1种ODS风险因素)【Clin J Am Soc Nephrol. 2018;13(7):984-992】。如果没有进行磁共振成像扫描,ODS可能诊断不足,尤其是那些无症状或症状轻微的人【Case Rep Neurol. 2012;4(3):167-172】。临床医生也可能低估了它的报告,因为它被认为是一种潜在的可预防并发症【Kidney Int Rep. 2018;3(1):24-35】。
由于ODS可能是一种破坏性后果,应谨慎避免过度纠正,以降低风险。因此,出于安全考虑,推荐的钠校正目标通常会偏于保守,特别是对于那些有ODS风险因素的患者,美国专家指南认可的每日校正限值为每24小时6至8 mmol/L(表3)。最重要的是pNa的24小时净变化,而不是精确的每小时修正率【Kidney Int. 1992;41(6):1662-1667】。 
支持性护理措施,如插管和通气,对于存活的患者,可能需要延长神经康复时间。当ODS发生时,对其进行优化管理是未来研究的一个重要领域。 预防ODS发生 在前述早期处理达到足以预防与ICP升高相关的急性结局的初始轻度钠升高后,重点转向预防钠进一步快速升高,以避免过度矫正和ODS。事实上,通常管理慢性(> 24小时)或持续时间未知的严重低渗性低钠血症的真正挑战,是防止这种潜在的有害过度治疗。可能需要使用静脉注射5%葡萄糖(伴或不伴去氨加压素)重新降低血清钠的作用,以降低尿量,通常在高依赖性环境(监护环境)中,以在24小时内将钠升高理想地维持在基线以上5-8 mmol,且在24小时内限制在不超过10-12 mmol(参见“过度纠正的情况下:重新降低血浆钠”)【Am J Med. 2013;126(10 Suppl 1):S1-42;EJE. 2014;170(3):G1-G47】。在有ODS风险因素的患者中(参见表2),校正速度应更慢,在24小时内校正4至6 mmol,在任何24小时内的校正限值为8 mmol/L【Am J Med. 2013;126(10 Suppl 1):S1-42;EJE. 2014;170(3):G1-G47】,尤其是因为这种增量通常足以预防与急性低钠血症相关的ICP升高的不良临床结局(参见“急性重度低钠血症”)。 已提出的另一种方法是“主动DDAVP”,即早期经验性联合使用去氨加压素(DDAVP)和高渗盐水【Am J Kidney Dis. 2013;61(4):571-578;Am J Kidney Dis. 2010;56(4): 774-779】。其基本原理是,过度纠正通常是短暂性SIAD消退、烦渴中断或致病药物停用后自发性水利尿的结果。这种自发性水清除可通过先发性去氨加压素【Farkas J. PulmCrit (EMCrit) 2015. Accessed July 28, 2022. https://emcrit.org/pulmcrit/taking-control-of-severe-hyponatremia- with-ddavp/】。这种方法的优点是,仅用高渗盐水(推注或输注)就可以更精确地控制校正率,无需应对可变输出。然而,在过度纠正发生或似乎即将发生之前通过给予AVP类似物来增强SIAD效应,这种方法存在低钠血症症状加重或延长的风险——尤其是在存在持续液体输入的情况下。在SIAD慢性病因患者(如SIAD副肿瘤患者)中,去氨加压素不太可能产生任何作用,因为抗利尿激素分泌的潜在原因可能会继续存在。这种前瞻性方法的唯一数据来自一项非对照的观察性研究,该研究对24例pNa低于120 mmol/L的患者进行,主要继发于噻嗪类利尿剂,每8小时用去氨加压素1至2 mcg治疗,并滴定基于体重的高渗盐水,使pNa在24小时内增加6 mmol/L。总体上,受试者在24小时内血清钠平均升高5.8 mmol/L,2例患者在4小时后血清钠下降1至2 mmol/L,2例患者在24小时内血清钠高于目标升高超过10 mmol/L,但未报告不良作用【Am J Kidney Dis. 2013;61(4):571-578】。目前没有足够的证据支持这一策略,相反,多数专家认可去氨加压素治疗的“反应性”或“抢救性”方法,符合当前指南。 另一种未广泛使用且多数情况下不推荐的急性重度低钠血症替代疗法,是通过中心静脉通路使用更高浓度的氯化钠(如23.4%或29.2% NaCl)。该治疗已被研究作为甘露醇的替代疗法,以提高创伤性脑损伤中的血浆张力,从而减少脑疝【Am J Med. 1982;72(1):43-48;Cochrane Database Syst Rev. 2019;12:CD010904;Neurology. 2008;70(13):1023-1029】。目前尚无低钠血症的质量数据来支持其使用,尤其是考虑到过度矫正的预期较高风险以及这些制剂外渗的潜在不良后遗症。 治疗严重低钠血症的潜在可逆性神经毒性,可能有助于阐明其对有多种潜在症状原因的患病患者的临床症状学(如意识状态改变)的贡献。如果症状在之前建议的适度pNa增量下没有改善,则应寻找替代或其他原因。 矫正过度:重新降低血浆钠 血清钠过度校正可能是任何钠升高干预的结果,也可能是随着AVP分泌的可逆刺激因素消退或停止过度水输入以及随后的脱水而自发发生的。没有证据表明慢性(> 48小时)低钠血症的自发性过度矫正比医源性过度矫正更安全。为了将校正率保持在目标范围内,可通过给予低渗液体、联合或不联合医源性AVP治疗(去氨加压素,DDAVP)以减少排尿来实现血清钠的“再既降低”(参见图4),并且当然停止任何积极的增加钠的治疗。由于ODS的症状会延迟数天,因此对无症状患者而言,重新降低血钠仍然至关重要,且也可能改善早期临床ODS患者的症状和结局【Clin J Am Soc Nephrol. 2020;15(2):282-284】。 开始重新降低钠的精确血清钠阈值尚未明确确定,可能取决于反映ODS风险的临床因素。欧洲指南建议在最初24小时内血清钠升高超过10 mmol/L,或在随后的24小时内升高超过8 mmol/L时,应立即进行干预,以重新降低【EJE. 2014;170(3):G1-G47】。美国专家小组建议,如果校正量超过10-12 mmol/L/天,则考虑对中度或低度ODS风险人群重新降低钠,但对于较高ODS风险人群(广义定义为pNa小于120 mmol/L,以及加上表2中的其他因素)的重新降低钠,在24小时内采用6至8 mmol/L的更保守阈值【Am J Med. 2013;126(10 Suppl 1):S1-42】。 血清钠的再降低是基于合理的生理学原理、临床前数据和人类病例系列;然而,RCT缺乏最佳策略的证据【Clin J Am Soc Nephrol. 2020;15(2):282-284】。在ODS的动物模型中,大鼠中的血清钠降低至115 mmol/L以下持续3天,然后用高渗盐水过度纠正(升高pNa > 25 mmol/L持续至少12小时),与仍持续大于20 mmol/L/天的更轻度纠正或没有纠正相比,用口服水丸重新降低以实现小于20 mmol/L/天的纠正梯度改善了ODS的死亡率和组织学严重程度 【Kidney Int. 1994;45(1):193-200;Kidney Int. 2009;76(6): 614-621】。事实上,所有24小时钠增加量被限制为小于20 mmol/L且具有再降低钠的大鼠都具有良好的神经学结局,但在20%中观察到轻度脑损伤,而在过度校正的对照大鼠中组织学脑损伤率为100%,死亡率为57%【Kidney Int. 1994;45(1):193-200】。
这些数据支持在ODS风险较高的人群中对pNa校正采用更严格的8-mmol/L限值,并支持一个合乎逻辑的结论,即虽然DDAVP可有效防止进一步升高,但也需要低渗液体来实现再灌注。 无电解质水给药(如口服水或静脉注射5%葡萄糖)对于控制过度矫正至关重要。欧洲指南建议在1小时内使用10 mL/kg的无电解质水(例如,对于50-100 kg的患者,在1小时内使用500-1000 mL)【EJE. 2014;170(3):G1-G47】。国际专家小组指南建议开始输注3 mL/kg/h的IV 5%葡萄糖(即,体重50-100 kg的患者为150-300 mL/h),并每小时监测一次,直至pNa恢复至24小时限值以下【Am J Med. 2013;126(10 Suppl 1):S1-42】。多数专家赞成根据欧洲指南增加前期追加量,然后在任何持续输注前进行重新评估。Adrogué-Madias公式可用于估计1000mL 5%葡萄糖的降钠作用,但需注意,该公式假设在使用葡萄糖时不会出现净无电解质水清除或滞留【NEJM. 2000;342(21):1581-1589】 (见图5)。如果pNa的上升速度超过预期,但尚未超过最大目标值,则可输注5%葡萄糖,以防止进一步升高。根据经验,在这种情况下,将液体输入速率与每小时尿液输出(无电解质水清除率的不完善指标)匹配应可稳定pNa。 去氨加压素是一种AVP类似物,可以静脉注射或皮下注射,剂量为1至2 mcg(微克),以减少尿量并防止pNa进一步增加【Am J Med. 2013;126(10 Suppl 1):S1-42;Am J Med. 2015;128(12):1362.e15-1362.e24;Clin J Am Soc Nephrol. 2008;3(2):331-336】。当对AVP的可逆性刺激不再存在且积聚的游离水正在迅速排泄(预示为低渗性多尿,即低UNa和渗透压)时,DDAVP对多尿患者特别有用。在这种情况下,与其通过尝试将尿量与高容积的5%葡萄糖或口服游离水相匹配来“追赶”多尿,不如减少尿量,允许可控地使用无电解质水以主动降低血清钠,通常是在密切监测的环境(如高依赖性或ICU)下,并密切进行血清钠监测(如1-2小时)。临床医生应注意,由于AVP受体阻滞,去氨加压素可能不能有效阻止托伐普坦的过度纠正,这取决于托伐普坦在肾集合管细胞的作用持续时间。DDAVP禁用于无法可靠限制摄入液体摄入的原发性烦渴患者。
尽管没有进行前瞻性比较,但一项后续回顾性研究(如前所述)得出结论,如果认为可能出现过度矫正,则应采取被动策略将pNa保持在目标范围内,这一结论得到了他们数据的最佳支持【Am J Med. 2018;131(3):317.e1-317.e10】。 总之,用不含电解质的水和/或DDAVP重新降低pNa的功能以实现安全的24小时净纠正是一个重要的工具,可能需要在通常精细的低钠血症管理过程中使用,以将不良结局的风险降至最低。 陈康 2023-12 |
- 上一篇:常见微生物抗感染治疗时应注意的天然耐药
- 下一篇:没有了